Автор:
Комаров Р.Н.1 , Виноградов О.А.1 , Яснопольская Н.В.1 , Дзюндзя А.Н.1 , Нагорный М.Н.2 1Клиника аортальной и сердечно-сосудистой хирургии (дир. – проф. Р.Н. Комаров) Первого МГМУ им. И.М. Сеченова; 2 отделение лучевой диагностики Первого МГМУ им. И.М. Сеченова, Москва, Россия
Источник:
ЖУРНАЛ: КАРДИОЛОГИЯ И СЕРДЕЧНО-СОСУДИСТАЯ ХИРУРГИЯ Издательство: Издательство Медиа Сфера (Москва) Том: 9Номер: 4 Год: 2016 Страницы: 81-85
Ключевые слова: посттравматическая артерио-венозная фистула, диагностика, хирургическое лечение.
В статье описан случай
хирургического лечения пациента с посттравматической артерио-венозной
фистулой между правой общей подвздошной артерией и нижней полой веной,
путем ее ушивания из просвета подвздошной артерии и последующей
пластикой артерии синтетической заплатой.
Диагноз артерио-венозного соустья
установлен на догоспитальном этапе по данным мультиспиральной
компьютерной томографии с контрастированием.
Целью нашего
сообщения является необходимость подчеркнуть диагностические трудности
при выявлении посттравматической артерио-венозной фистулы, тяжесть
патоморфологических изменений и осложнений связанных с наличием
массивного артерио-венозного сброса, необходимость раннего выявления и
хирургической коррекции данного состояния.
Введение
Повреждения магистральных сосудов в
мирное время составляют 3% от других травм, которые в свою очередь
занимают лидирующие позиции среди причин смертности, особенно среди лиц
молодого и трудоспособного возраста. [5] Большая медико-социальная
значимость данной проблемы не вызывает сомнений, так как 5% летальность
при повреждениях магистральных сосудов достаточно высокий показатель,
учитывая уровень развитие современной медицины. [1] Ошибки первичной
диагностики закрытых травм сосудов, по данным различных источников
составляют от 50 до 70%. Они происходят вследствие неадекватной ревизии
раны во время первичной хирургической обработки. В последствии эти
ошибки приводят к формированию посттравматических аневризм и
артерио-венозных сообщений. [5] Высокие артерио-венозные фистулы, такие
как аорто-кавальные или подвздошно-кавальные, в 80 - 90% случаев
являются результатом аррозии стенки аневризмы аорты или разрыва
аневризмы в нижнюю полую вену. Остальные 10-20% - результат проникающего
ранения брюшной полости или же ятрогенной травмы. [6] Большинство
больных с проникающими ранениями и травмой сосудов не доживают до
момента госпитализации по причине массивной кровопотери. В тех случаях,
когда пациента успевают доставить в клинику, интра- и послеоперационная
летальность приближается к 50%. [4,7] Значительно реже такого рода
повреждения сопровождаются закрытой травмой сосудов и в дальнейшем
приводят к формированию высоких артерио-венозных фистул, которые
манифестируют клиникой нарастающей сердечной недостаточности.
Длительность компенсации, сроки развития клиники сердечной
недостаточности напрямую зависят от уровня расположения фистулы
относительно сердца, ее размеров, длительности существования соустья и
возраста пациента. В литературе имеются единичные публикации,
посвященные непосредственно посттравматическим соустьям. Патофизиология
изменений происходящих при выраженном артерио-венозном сбросе
характеризуется формированием патологического дополнительного круга
кровообращения, так называемого «фистулезного», в результате которого
происходит изменение центральной и регионарной гемодинамики. [2]
Изменения центральной гемодинамики заключаются в перегрузке правых
отделов сердца объемом и развитии клиники правожелудочковой
недостаточности. Единственный способ лечения - хирургическая коррекция
данной патологии, которая сопряжена с рядом технических проблем,
обусловленных предшествующим хирургическим вмешательством и развитием
рубцово-спаечного процесса в этой области, изменением анатомии области
хирургического интереса и высоким риском интраоперационной кровопотери. В
настоящее время нет единого мнения, четких рекомендаций и тактики
ведения данной группы пациентов. Имеются публикации, сообщающие о 30%
летальности при открытом хирургическом лечении данной группы больных,
преимущественно за счет массивной кровопотери [3]. С внедрением
мини-инвазивных методик и развитием эндоваскулярной хирургии открылись
новые горизонты в лечении. Они дают возможность минимизировать
хирургическую травму, избежать трудностей связанных с повторным
вмешательством на предполагаемой зоне, тяжелых осложнений, а так же
сократить сроки пребывания в стационаре и период реабилитации. Однако
эти «идеальные» во всех отношениях операции имеют ряд технических
ограничений, не позволяющих использовать данный метод во всех
клинических случаях.
Клинический случай
В данной публикации описан случай
успешного хирургического разобщения артерио-венозной фистулы,
сформированной в результате проникающего ножевого ранения брюшной
полости и не ликвидированного на этапе первичного хирургического
вмешательства. Пациент был оперирован через 1,5 года после ранения в
отделении сосудистой хирургии Клинки аортальной и сердечно-сосудистой
хирургии Первого МГМУ им. И.М. Сеченова.
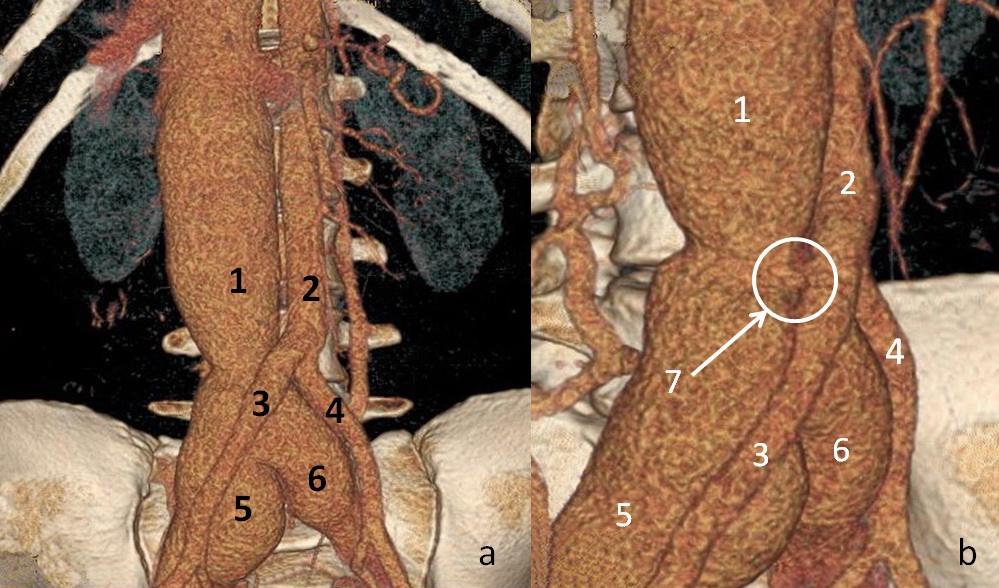
Рисунок 1.
МСКТ брюшной аорты с
контрастированием: а. - 3D реконструкция (Volume Rendering); b. –
увеличенный фрагмент 3D реконструкции (Volume Rendering); .
1. - расширенная
нижняя полая вена; 2. – инфраренальный отдел брюшной аорты; 3. – правая
общая подвздошная артерия; 4. – левая общая подвздошная артерия; 5. –
расширенная правая общая подвздошная вена; 6. – расширенная левая общая
подвздошная вена; 7. – артерио-венозная фистула;
Больной П., 32 лет, поступил в
отделение с диагнозом: артерио-венозная фистула со сбросом крови из
правой общей подвздошной артерии в нижнюю полую вену (по данным
мультиспиральной компьютерной томографии (МСКТ) аорты и артерий нижних
конечностей с контрастированием на догоспитальном этапе), для планового
оперативного лечения. На момент госпитализации предъявлял жалобы на
общую слабость, одышку при незначительной физической нагрузке,
тахикардию, увеличение живота в объеме, отечность нижних конечностей.
История заболевания начинается с момента получения пациентом ножевого
ранения в феврале 2014 года, по поводу чего в экстренном порядке был
госпитализирован и оперирован в хирургическом стационаре. Одно входное
отверстие локализовалось на 3 см выше пупка по средне-ключичной линии на
границе околопупочной и правой боковой областей живота, второе - в
поясничной области справа. При ревизии органов брюшной полости выявлено
сквозное ранение восходящей ободочной кишки, в связи с чем было
произведено ушивание ее дефекта, других повреждений выявлено не было. С
сентября 2014 года пациент стал отмечать слабость, утомляемость, в
последствие к которым присоединилась одышка при физической нагрузке,
тахикардия, а в дальнейшем явления асцита и периферические отеки.
Неоднократно получал лечение в кардиологических стационарах, где
основным диагнозом был инфекционно-аллергический миокардит, а с марта
2015 года выставлен диагноз - дилатационная кардиомиопатия. Дважды
производился лапароцентез с эвакуацией более 5 литров асцитической
жидкости. Однако проводимое лечение не давало клинического улучшения.
Диагноз был установлен после проведения МСКТ брюшной полости с
контрастированием аорты и артерий нижних конечностей, по результатам
которого выявлено наличие у пациента артерио-венозного сброса из правой
общей подвздошной артерии в нижнюю полую вены с ее расширением до 52 мм
(рис. 1, 2). По данным эхокардиографии - дилатация всех камер сердца:
правое предсердие 141 мл, правый желудочек 4,1 см; дилатация ствола
легочной артерии до 4,2 см, признаки легочной гипертензии - СДЛА в
легочной артерии более 50 мм. рт. ст. Нижняя полая вена расширена на
уровне впадения в правое предсердия до 3,6 см, спадение ее на вдохе
менее 30%. Конечный диастолический объем (КДО) левого желудочка
составлял 194 мл, размер левого предсердия - 4,8 см. После верификации
диагноза пациент консультирован сердечно-сосудистым хирургом и
госпитализирован в Клинику аортальной и сердечно-сосудистой хирургии
Первого МГМУ им. И.М. Сеченова.
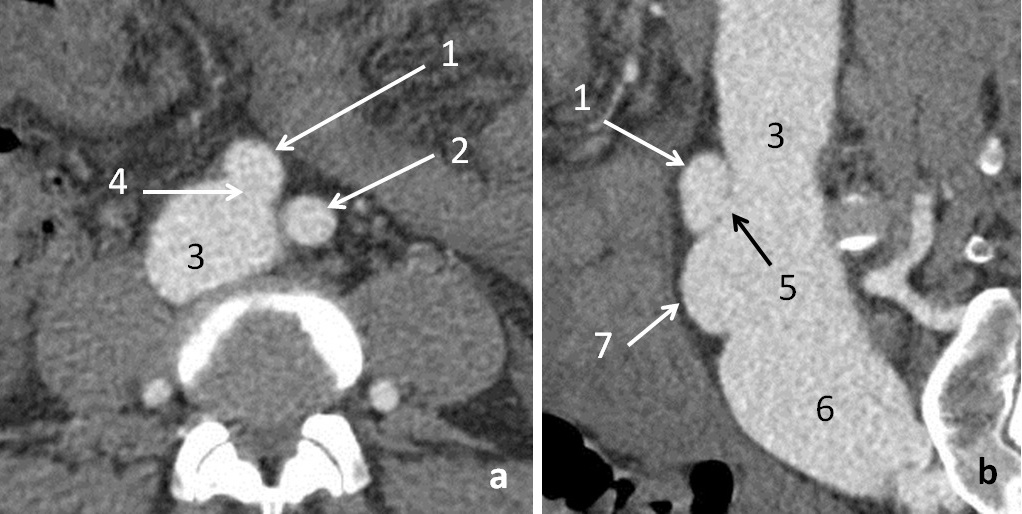
Рисунок 2.
МСКТ брюшной аорты с
контрастированием: а. - поперечный срез, увеличенный фрагмент; b. –
мультипланарная реконструкция, косая проекция.
1. – правая общая
подвздошная артерия; 2. – левая общая подвздошная артерия; 3. - нижняя
полая вена; 4. – артерио-венозная фистула (поперечный размер фистулы 14
мм); 5. - артерио-венозная фистула (продольный размер фистулы 8 мм); 6. –
левая общая подвздошная вена; 7. – правая общая подвздошная вена;
В клинике было принято решение о
необходимости устранения патологического артерио-венозного сброса
хирургически. Пациент оперирован 12 февраля 2016 года. После выполнения
полной срединной лапаротомии, вскрытия брюшной полости одномоментно
эвакуировано более 7 литров асцитической жидкости соломенно-желтого
цвета. При ревизии инфраренальный отдел аорты (1,8 см) и левая общая
подвздошная артерия (0,9 см) нормального диаметра, правая общая
подвздошная артерия (ОПА) несколько ротирована кпереди и расширена до
1,2 см. Правая латеральная стенка аорты, а также латеральная и задняя
стенки правой общей подвздошной артерии интимно спаяны с расширенной
нижней полой веной, над которой определялся грубый
систоло-диастолический шум и активная пульсация. Кроме того в этой зоне
наблюдался выраженный рубцовый процесс, в связи с чем выделение нижней
полой вены (НПВ) технически не представлялось возможным (рис. 3).
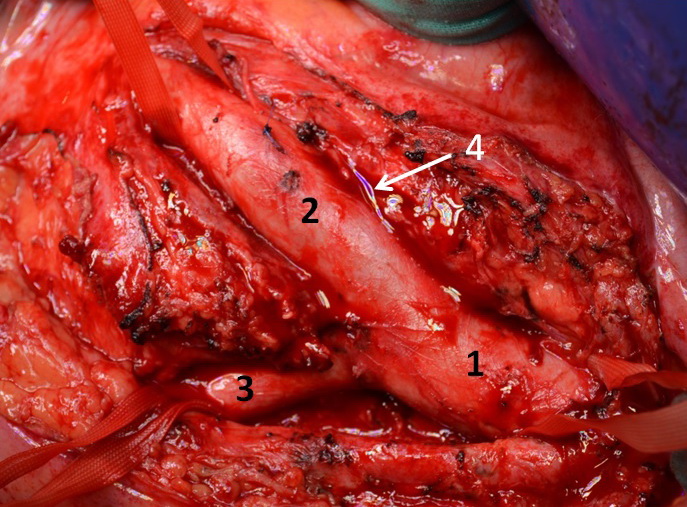
Рисунок 3.
Интраоперационная
фотография: 1. – инфраренальный отдел аорты; 2. – правая общая
подвздошная артерия; 3. - левая общая подвздошная артерия; 4. – место
проекции артерио-венозной фистулы (систоло-диастолический шум);
После пережатия аорты и
подвздошных артерий, прижатия НПВ марлевыми тупферами, произведена
продольная аорто-артериотомия с переходом на правую ОПА, после чего
получено активное поступление крови из соустья. Дефект был обтурирован
путем введения катетера Фолея 24F через артерио-венозное сообщение в
просвет НПВ с последующим раздуванием баллона. Таким образом,
кровотечение было временно остановлено. При ревизии выявлено, что
дефект, диаметром 0,8 х 1,4 см, располагался на расстоянии 2 см от
уровня бифуркации аорты (рис. 4).
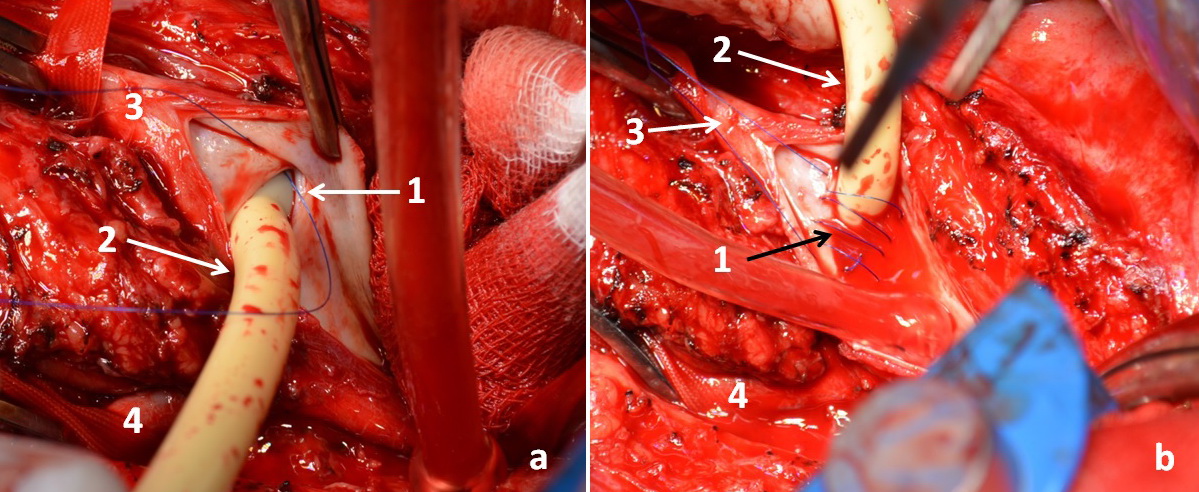
Рисунок 4.
а. -
интраоперационная фотография; b. – интраоперационная фотография (перед
удалением катетера Фолея и затягиванием ниток): 1. – артерио-венозная
фистула из просвета правой общей подвздошной артерии; 2. - катетер Фолея
24 F; 3. – правая общая подвздошная артерия; 4. – левая общая
подвздошная артерия.
Ушивание соустья производилось из
просвета артерии, путем наложения непрерывного обвивного шва нитью
пролен 4/0, предварительно не затягивая нити. С последним швом катетер
Фолея удален, швы затянуты, артерио-венозное соустье разобщено.
Аорто-артериотомия ушита при помощи синтетической заплаты из ПТФЕ, пущен
кровоток (рис. 5).
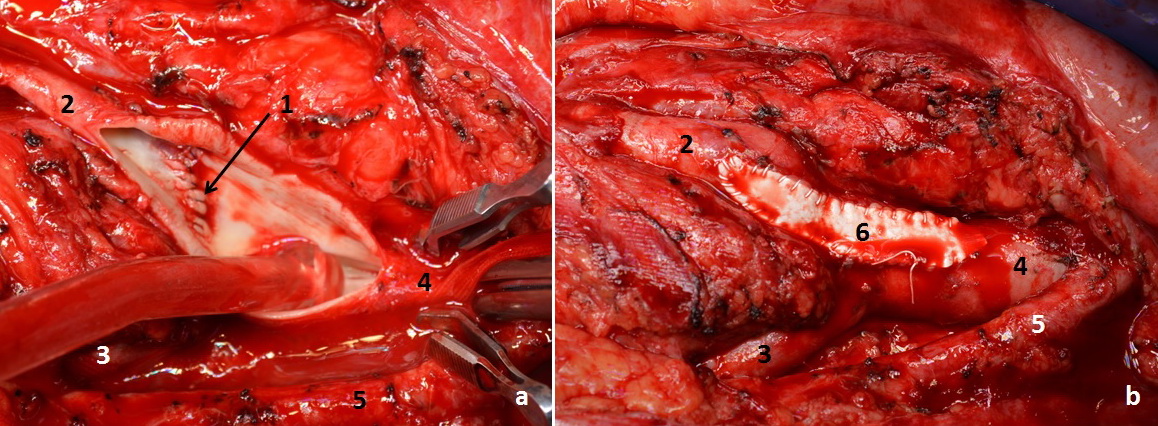
Рисунок 5.
а. -
интраоперационная фотография (ушитая артерио-венозная фистула); b. –
интраоперационная фотография (пластика аорто-артериотомии): 1. –
артерио-венозная фистула ушитая из просвета правой общей подвздошной
артерии; 2. - правая общая подвздошная артерия; 3. – левая общая
подвздошная артерия; 4. – инфраренальный отдел аорты; 5. – нижняя
брыжеечная артерия; 6. - пластика аорто-артериотомии заплатой из ПТФЭ;
Время пережатия аорты составило 35
мин. Объем кровопотери составил 4000 мл, который был компенсирован 3
дозами донорской крови и 3 дозами плазмы, а также реинфузией отмытых,
при помощи аппарата Cell Saver, эритроцитов в объеме 2100 мл. После
завершения операции пациент был экстубирован и в стабильном состоянии
переведен в отделение реанимации. Контроль МСКТ ангиографии выполнен на 5
сутки (рис. 6).
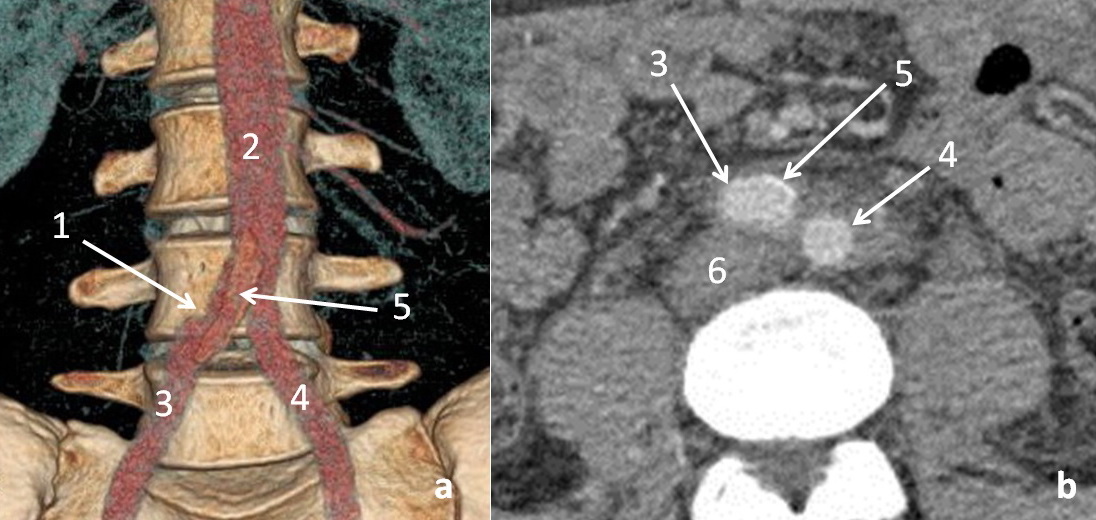
Рисунок 6.
МСКТ брюшной аорты с
контрастированием: а. - 3D реконструкция (Volume Rendering) –
отсутствует контрастирование системы нижней полой вены; b. - поперечный
срез, увеличенный фрагмент;
1.- место проекции
ушитой артерио-венозной фистулы; 2. - инфраренальный отдел аорты; 3. -
правая общая подвздошная артерия; 4. - левая общая подвздошная артерия;
5. - пластика аорто-артериотомии заплатой из ПТФЭ; 6. – уменьшившаяся в
размере нижняя полая вена;
Данных за артерио-венозный сброс
не получено. Наблюдается уменьшение размеров нижней полой до 24-32 мм и
подвздошных вен до 18 мм справа и 16 мм слева. Отсутствуют признаки
наличия свободной жидкости в брюшной полости. По данным контрольной
эхокардиографии на 6 сутки установлена положительная динамика в виде
тенденции к уменьшению камер сердца: правое предсердие – 98 мл, правый
желудочек 3,8 см, левое предсердие 4,5 см. КДО 150 мл. Отмечается
тенденция к снижению давления в легочной артерии - СДЛА 34 мм. рт. ст.
Степень регигургитации на трикуспидальном клапане уменьшилась до 1
степени. Диаметр НПВ на уровне впадения в правое предсердие 2 см. С
клиническим улучшением пациент выписан из отделения на 14 сутки.
Заключение.
Наличие патологического
артерио-венозного сообщения приводит к тяжелой, плохо поддающейся
коррекции, а порой необратимой сердечной недостаточности. На сегодняшний
день в литературе встречаются единичные публикации о лечении высоких
посттравматических артерио-венозных фистул. Вероятно, это обусловлено
тем, что ранение магистральных сосудов и формирование хронических форм
повреждения более актуально для артерий верхних и нижних конечностей, в
то время как ранение крупных артериальных и венозных магистралей брюшной
полости завершается профузным кровотечением, которое приводит к гибели
больного. Формирование артерио-венозных фистул является результатом
закрытых сосудистых повреждений, дефектом ранней диагностики и
неадекватной ревизией сосудов во время первичного хирургического
вмешательства, поэтому со времени получения травмы до момента установки
диагноза артерио-венозной фистулы проходит зачастую не один год.
Клиническая картина скрывается за маской сердечной декомпенсации, как
проявления системных гемодинамических изменений, а в случае преобладания
регионарных нарушений - под маской хронической венозной недостаточности
или артериальной недостаточности. При этом пациенты годами получают
лечение, которое не приносит результата, так как правильный диагноз
зачастую отсутствует. Наиболее точными способами диагностики являются:
МСКТ с контрастированием, прямая ангиография и ультразвуковое
триплексное сканирование. Настороженность хирургов общего профиля -
залог своевременной диагностики и устранения сосудистого повреждения.
Раннее выявление и хирургическое лечение хронических форм сосудистой
травмы с артерио-венозным сбросом дает возможность избежать необратимых
гемодинамических изменений, уменьшению выраженности приобретенной
сердечной недостаточности и как следствие улучшению качества и
продолжительности жизни больного.
Список литературы:
|
1.Бочаров С.М. Ангиографическая диагностика и эндоваскулярное лечение при травме артерий/ С.М. Бочаров – Москва, 2009.
2.Чернуха Л.М., Никульников П.И.,
Каширова Е.В., Влайков Г.Г., Альтман И.В., Гуч А.А., Матящук А.С.
Посттравматические артериовенозные фистулы. Опыт лечения. Новости
хирургии. 2011; 19:3:63-69.
3.Brightwell RE, Pegna V, Boyne N.
Aortocaval fistula: current management strategies. ANZ journal of
surgery. 2013 Jan; 83(1-2):31-5. DOI:10.1111/j.1445-2197.2012.06294.x
4.Carrillo E.H., Bergamini, T.M., Miller, F.B., and Richardson, J.D. Abdominal vascular injuries. J Trauma. 1997; 43: 164–171.
5.Coimbra, R. Epidemiology of
vascular trauma / R. Coimbra, D. B. Hoyt. // Vascular surgery / Eds. R.
B. Rutherford. – 2005. – Vol. 2. – 1001 p.
6.Davidovic L.B., Kostic D.M.,
Cvetkovic S.D., Jakovljevic N.S., Stojanov, P.L., Kacar A.S. et al.
Aorto-caval fistulas. Cardiovasc Surg. 2002; 10: 555–560.
7.Feliciano D.V., Burch J.M. and
Graham J.M. Abdominal vascular injury. In: D.V. Feliciano, E.E. Moore,
K.L. Mattox (Eds.) Appleton & Lange, Trauma. Norwalk (CT); 1996:615.
|
1.Bocharov S.M. Angiograficheskaya diagnostika i endovaskulyarnoe lechenie pri travme arterii/ S.M. Bocharov – Moskva, 2009.
2.Chernukha L.M., Nikul'nikov P.I.,
Kashirova E.V., Vlaikov G.G., Al'tman I.V., Guch A.A., Matyashchuk A.S.
Posttravmaticheskie arteriovenoznye fistuly. Opyt lecheniya. Novosti
khirurgii. 2011; 19:3:63-69.
3.Brightwell RE, Pegna V, Boyne N.
Aortocaval fistula: current management strategies. ANZ journal of
surgery. 2013 Jan; 83(1-2):31-5. DOI:10.1111/j.1445-2197.2012.06294.x
4.Carrillo E.H., Bergamini, T.M., Miller, F.B., and Richardson, J.D. Abdominal vascular injuries. J Trauma. 1997; 43: 164–171.
5.Coimbra, R. Epidemiology of
vascular trauma / R. Coimbra, D. B. Hoyt. // Vascular surgery / Eds. R.
B. Rutherford. – 2005. – Vol. 2. – 1001p.
6.Davidovic L.B., Kostic D.M.,
Cvetkovic S.D., Jakovljevic N.S., Stojanov, P.L., Kacar A.S. et al.
Aorto-caval fistulas. Cardiovasc Surg. 2002; 10: 555–560.
7.Feliciano D.V., Burch J.M. and
Graham J.M. Abdominal vascular injury. In: D.V. Feliciano, E.E. Moore,
K.L. Mattox (Eds.) Appleton & La nge, Trauma. Norwalk (CT);
1996:615.
|
« Все статьи